EKSKLUZIVNO ISTRAŽIVANJE
Genetski modificirani ‘Magneto’ protein daljinski kontrolira mozak i ponašanje

Znanstveni magazin „Nature Neuroscience“ objavio je 29.05. 2023. rezultate eksperimentalnih istraživanja grupe neuroznanstvenika o magnetiziranom proteinu, konstruiranom genetskim inženjeringom, koji omogućava daljinsko aktiviranje određenih grupa moždanih stanica.
O tome je izvjestio The Guardian, čiji članak prenosimo u cijelosti:
Genetski modificirani ‘Magneto’ protein daljinski kontrolira mozak i ponašanje
„Zločesta“ nova metoda koristi magnetizirani protein za brzo, reverzibilno i neinvazivno aktiviranje moždanih stanica
Istraživači u Sjedinjenim Američkim Državama, koristeći genetski inženjering za stvaranje magnetiziranog proteina koji daljinski aktivira određene skupine živčanih stanica, razvili su novu metodu za kontrolu dijelova mozga, povezanih sa složenim ponašanjem životinja.
Razumijevanje načina na koji mozak stvara ponašanje jedan je od najvažnijih ciljeva neuroznanosti – i jedno od njezinih najtežih pitanja. Posljednjih godina istraživači su razvili niz metoda koje im omogućuju daljinsko upravljanje određenim skupinama neurona i ispitivanje rada neuronskih veza.
Najmoćnija od njih je metoda nazvana optogenetika,(optogenetics) koja omogućava istraživačima uključivanje ili isključivanje grupa srodnih neurona milisekundu po milisekundu na vremenskoj skali, pomoću impulsa laserskog svjetla.
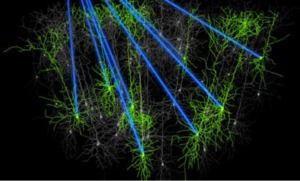
Utjecaj svjetlom na moždane aktivnosti (Researchers read and write brain activity with light | Science | The Guardian)
Druga nedavno razvijena metoda, nazvana kemogenetika, (chemogenetics) koristi konstruirane proteine koji se aktiviraju dizajniranim lijekovima i koji se mogu usmjeriti na specifične tipove stanica.
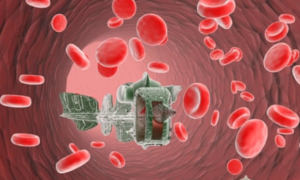
Daljinska kontrola moždanih aktivnosti pomoću zagrijanih nanočestica (Remote control of brain activity with heated nanoparticles | Science | The Guardian)
Iako su moćne, obje ove metode imaju nedostatke. Optogenetika je invazivna, zahtijeva umetanje optičkih vlakana koja isporučuju svjetlosne impulse u mozak, a kod toga je ozbiljno ograničen opseg do kojeg svjetlost prodire kroz gusto tkivo mozga. Kemogenetski pristupi nadilaze oba ova ograničenja, ali obično induciraju biokemijske reakcije kojima je potrebno nekoliko sekundi da bi aktivirale živčane stanice.
Nova tehnika, razvijena u laboratoriju Alija Gülera (Ali Güler’s lab) na Sveučilištu Virginia, Charlottesville, te opisana u gore navedenoj publikaciji objavljenoj u magazinu Nature Neuroscience, ne samo da nije invazivna, već brzo i reverzibilno može aktivirati neurone.
Nekoliko ranijih studija pokazalo je da se proteini živčanih stanica, koji se aktiviraju toplinom i mehaničkim pritiskom, mogu genetski modificirati tako da postanu osjetljivi na radio valove (Remote control of ion channels and neurons through magnetic-field heating of nanoparticles | Nature Nanotechnology) i magnetska polja (Selective activation of mechanosensitive ion channels using magnetic particles – PMC (nih.gov)), pričvršćujući ih na protein koji skladišti željezo, nazvan feritin ili na anorganske paramagnetske čestice. Ove metode predstavljaju važan napredak – primjerice, već su korištene za regulaciju razine glukoze u krvi kod miševa (Remote regulation of glucose homeostasis in mice using genetically encoded nanoparticles | Nature Medicine) – ali uključuju više komponenti koje se moraju uvesti odvojeno.
Ova nova tehnika temelji se na ovom ranijem radu, a temelji se na proteinu zvanom TRPV4, koji je osjetljiv i na temperaturu i na sile istezanja (Wild-type and Brachyolmia-causing Mutant TRPV4 Channels Respond Directly to Stretch Force – PMC (nih.gov)). Ovi podražaji otvaraju njegovu središnju poru, dopuštajući električnoj struji da teče kroz staničnu membranu; ovo izaziva živčane impulse koji putuju u leđnu moždinu i potom do mozga.
Güler i njegovi kolege zaključili su da sile magnetskog zakretnog momenta (ili rotacije) mogu aktivirati TRPV4 otvaranjem njegove središnje pore, pa su upotrijebili genetski inženjering za spajanje proteina s paramagnetskim područjem feritina, zajedno s kratkim sekvencama DNK koje signaliziraju stanicama transport proteina na membranu živčane stanice i umetanje u nju.
Kada su uveli ovaj genetski konstrukt u stanice bubrega ljudskog embrija koje su rasle u Petrijevim zdjelicama, stanice su sintetizirale ‘Magneto’ protein i umetnule ga u svoju membranu. Primjena magnetskog polja aktivirala je projektirani protein TRPV1, što je dokazano prolaznim povećanjem koncentracije kalcijevih iona unutar stanica, a to je pokazano fluorescentnim mikroskopom.
Zatim su istraživači umetnuli Magneto DNA sekvencu u genom virusa, zajedno s genom koji kodira zeleni fluorescentni protein i regulatorne DNA sekvence koje uzrokuju ekspresiju konstrukta samo u određenim vrstama neurona. Nakon toga su ubrizgali virus u mozgove miševa, ciljajući na entorinalni korteks, i secirali mozgove životinja kako bi identificirali stanice koje emitiraju zelenu fluorescenciju. Koristeći mikroelektrode, zatim su pokazali da primjena magnetskog polja na rezove mozga aktivira Magneto tako da stanice proizvode nervne impulse.
Kako bi utvrdili može li se Magneto koristiti za manipuliranje neuronskom aktivnošću kod živih životinja, ubrizgali su Magneto u ličinke zebrice, ciljajući neurone u trupu i repu koji inače kontroliraju reakciju bijega. Potom su stavili ličinke zebrice u posebno izgrađeni magnetizirani akvarij i otkrili da je izloženost magnetskom polju inducirala manevre „namotavanja u zavojnice“, slične onima koji se javljaju tijekom reakcije bijega. (Ovaj eksperiment uključio je ukupno devet ličinki zebrice, a naknadne analize otkrile su da svaka ličinka sadrži oko 5 neurona koji eksprimiraju Magneto.)
https://youtu.be/iHTpJNSNFlc (From Wheeler et al 2016)
U završnom eksperimentu, istraživači su ubrizgali Magneto u striatum miševa koji se slobodno ponašaju, odnosno u duboku moždanu strukturu koja sadrži neurone koji proizvode dopamin i koji su uključeni u nagrađivanje i motivaciju. Zatim su životinje stavili u aparat podijeljen na magnetizirane i nemagnetizirane dijelove. Miševi koji su eksprimirali Magneto proveli su daleko više vremena u magnetiziranim područjima nego miševi koji nisu, jer je aktivacija proteina uzrokovala da strijatalni neuroni koji ga eksprimiraju otpuštaju dopamin, tako da su miševi smatrali kako je boravak u tim područjima nagrada. To pokazuje da Magneto može daljinski kontrolirati aktiviranje neurona duboko u mozgu, te također kontrolirati složena ponašanja
Neuroznanstvenik Steve Ramirez
sa Sveučilišta Harvard, koji koristi optogenetiku za manipulaciju sjećanjima u mozgovima miševa, kaže kako je ova nova studija “zločesta”.
“Prijašnji pokušaji [korištenja magneta za kontrolu aktivnosti neurona] zahtijevali su višestruke komponente za rad sustava – ubrizgavanje magnetskih čestica, ubrizgavanje virusa koji eksprimira kanal osjetljiv na toplinu, [ili] fiksiranje glave životinje kako bi zavojnica mogla inducirati promjene u magnetizmu”, objašnjava on.
“Problem s višekomponentnim sustavom je taj što postoji toliko prostora da se svaki pojedinačni dio može razgraditi.”
“Ovaj sustav ima jedan elegantan virus koji se može ubrizgati bilo gdje u mozak, što ga čini tehnički lakšim i manje vjerojatnim da će ga pokvariti pokretna zvona i zviždaljke “, te dodaje
“bihevioralna oprema je pametno i prikladno dizajnirana da sadrži magnete kako bi se životinje mogle slobodno kretati.”
„Magnetogenetika” je stoga važan dodatak oruđu neuroznanstvenika, koji će se nedvojbeno dalje razvijati i pružiti istraživačima nove načine proučavanja razvoja i funkcije mozga.
Reference
Wheeler, M. A., et al. (2016). Genetically targeted magnetic control of the nervous system. Nat. Neurosci., DOI: 10.1038/nn.4265 [Abstract]
HOP na Telegramu
Telegram kanal Arna Šebalj:













